Introduction
A la suite de différentes crises et devant la préoccupation croissante concernant les risques chroniques émergeants, un cadre structuré a été proposé aux Etats-Unis, en 1983, pour encadrer la mobilisation des connaissances scientifiques en tant qu’aide à la décision publique. Ce cadre, avec ses différentes étapes, de la recherche jusqu’à la gestion du risque, est progressivement devenu (avec des adaptations) la référence sur le plan international. Ce cours introductif présente la phase d’évaluation du risque, celle qui correspond à la mise en œuvre de l’expertise scientifique, de l’identification du danger, à la caractérisation du risque. Le cours fait donc référence à la santé environnementale, autre domaine complexe et de reconnaissance relativement récente, même si chez les
hygiénistes du 19ème siècle on trouve déjà les prémices de cette démarche.
Après une partie introductive consacrée, entre autres, à une série de définitions, nous exposerons les principales approches disciplinaires : toxicologie, expologie et épidémiologie. La deuxième partie sera consacrée à la typologie des facteurs de risque et des circonstances d’exposition qui génèrent les risques. Des exemples illustreront les différentes classifications.
Remarque
Extrait du rapport au National Research Council : “…une démarche méthodique de synthèse des connaissances scientifiques disponibles en vue d’évaluer les effets sur la santé résultant d’une exposition d’une population ou d’individus à une substance, un agent ou une situation dangereuse ;”
National Academy of Science (USA), 1983.
Quelques réflexions sur les causes des états pathologiques
Dans les dernières années nos connaissances fondamentales sur les causes des grandes maladies ont beaucoup évolué. Nous ne pouvons ignorer leur complexité qui se retrouve dans la multiplicité des causes, mais aussi dans les différents mécanismes moléculaires à l’origine de pathologies en apparence similaires. Ainsi, prétendre que la “cause” d'une pathologie réside dans une “exposition” à un facteur unique, c'est méconnaître la nature biologique des phénomènes. La plupart des maladies résultent d'une combinaison :
-
d'expositions à des facteurs déterminants ;
-
de l'influence d'autres facteurs environnementaux, qualifiés de modificateurs ;
-
de facteurs héréditaires dits de susceptibilité ;
-
mais aussi d'une certaine part de hasard.
L'étude de la santé des populations se doit d'intégrer cette complexité. Mais il nous faut aussi avoir présente à l'esprit la notion plus dynamique de l'interaction entre les lois de l'évolution, dans le sens darwinien et les modifications de notre environnement d'origine anthropique. Ce principe s'applique à l'analyse de l'évolution de nombreuses pathologies importantes comme le cancer, mais aussi certaines maladies infectieuses, ainsi que l'obésité ou le diabète. L'adaptation physiologique de notre organisme peut-elle suivre la rapidité avec laquelle nous modifions notre environnement ?
Il s’agit de notre santé, mais aussi de l’environnement
La définition de la santé la plus couramment utilisée est celle qui a été adoptée par l'OMS en 1946. Elle indique que “la santé est un état de complet bien-être physique, mental et social, et ne consiste pas seulement en une absence de maladie ou d'infirmité”. Plus récemment la charte d'Ottawa du 21 novembre 1986 adoptée par les deux bureaux de l'OMS Europe - promotion de la santé et environnement - mentionne que “la santé constitue la mesure dans laquelle un individu ou un groupe est apte à réaliser ses aspirations et à satisfaire ses besoins et d'autre part à s'adapter à son environnement et à le modifier”.
Si cette approche globale a le mérite d'intégrer les composantes sociales et psychologiques de la santé, il est à l'évidence difficile de préciser les caractéristiques objectives d'un état de «complet bien-être» que certains auteurs ont critiqué comme pouvant être assimilé à la définition du bonheur.
Remarque
"La santé environnementale (environmental health) comprend les aspects de la santé humaine, y compris la qualité de vie, qui sont déterminés par les facteurs physiques, chimiques, biologiques, sociaux, psychosociaux et esthétiques de notre environnement. Elle concerne également la politique et les pratiques de gestion, de résorption, de contôle et de prévention des facteurs environnementaux susceptibles d'affecter la santé des générations actuelles et futures"
Pour ce qui concerne la santé environnementale, nous retiendrons ici la définition proposée par le bureau européen de l'Organisation mondiale de la santé (OMS) lors de la conférence d'Helsinki de 1994 (cf. ci-contre). Elle a l'avantage de s'accorder avec la définition de la santé, adoptée par la même OMS en 1946. Il reste alors à préciser la définition de l'environnement qui, force est de constater, varie également selon les interlocuteurs et les points de vue. La teneur de la définition est loin d'être anodine quant à la portée du discours [Quand certains déclarent que 80% des cancers trouvent leurs causes dans l'environnement, il faut comprendre que seuls 20% des cancers ont une composante héréditaire]. Ces notions sont très importantes pour apprécier les disparités des statistiques issues de sources différentes. Il faut aussi reconnaître le caractère éminemment multidisciplinaire de la santé environnementale, qui fait appel à des spécialités typiquement du domaine de la santé (épidémiologie, toxicologie, entre autres), comme des sciences humaines (économie, droit, sociologie).
Danger et risque une distinction essentielle
Une substance, un produit ou une circonstance [Une activité ou un élément du mode de vie, une profession ou le tabagisme par exemple] peuvent être reconnus dangereux. Cependant, pour que l’on puisse établir une probabilité d’occurrence d’un dommage sanitaire, il faut que les personnes soient exposées au danger. A chaque niveau d’exposition il est théoriquement possible de calculer une probabilité qui représente le risque de développer l’état pathologique. Il nous faut donc distinguer danger et risque dans le but de pouvoir prendre des décisions, sous forme de recommandations ou de règles contraignantes, pour limiter le risque et non pour agir sur le danger. La gestion du risque consistera dès lors à prendre des mesures appropriées et proportionnelles en fonction du niveau de risque tel qu'il a été évalué par les moyens que nous définirons plus loin.
De même, ayant fait la distinction, il est facile de comprendre que le processus d’évaluation des risques débute avec l’identification des dangers, propriétés (nature corrosive, inflammable) et types de toxicité par exemple. Ainsi, se dessine le cadre de l’évaluation des risques avec le positionnement des différentes disciplines qui y contribuent.
Principales contributions disciplinaires
La toxicologie, discipline au cœur de la caractérisation du danger
Selon le GATOX, (Septembre 2001), le champs d'investigation de la toxicologie peut être présenté de la façon suivante :
“
La toxicologie s'intéresse particulièrement à l'identification du danger et à l'analyse du risque lié à l'exposition des organismes vivants aux xénobiotiques, littéralement substance étrangère au corps, donc pas nécessairement toxique (agents chimiques, physiques, et d'origine biologique) dans le but de définir la sécurité sanitaire des populations. A cet effet, la toxicologie développe et utilise des modèles expérimentaux moléculaires, cellulaires et intégrés ainsi que des modèles bio-informatique”.
La toxicité se défini comme toute manifestation pathologique observable au niveau de l’organisme vivant étudié et attribuable à l’agent administré dans des conditions expérimentales contrôlées. Le terme organisme vivant est utilisé ici dans un sens large. Il peut s’agir de différentes espèces animales ou végétales, voire de cellules en cultures.
Quant aux déterminants toxiques, on admet généralement qu’il s’agit de facteurs physiques, chimiques ou biologiques. Des exemples seront donnés dans la suite.
La notion qui se trouve au centre de l’étude toxicologique est celle de la relation dose-effet. Ceci peut être interprété de deux façons :
-
Des déterminants auxquels nous sommes exposés en permanence peuvent s’avérer toxiques à forte dose (le cas du sel de cuisine par exemple).
-
A contrario, pour un toxique donné (n’importe quel poison) il existe un seuil au dessous duquel il n’y aura aucune manifestation pathologique.
Remarque
Les manifestations toxiques se divisent grossièrement en deux types :
- La toxicité d’organe, dans le cas où les effets se produisent préférentiellement dans un organe comme le foie (hépatotoxicité), ou dans un système (système nerveux = neurotoxicité) ;
- La toxicité systémique pour tout effet qui concerne l’ensemble des cellules et tissus d’un organisme donné, l’exemple étant la génotoxicité (atteinte du patrimoine génétique avec altération de la séquence de l’ADN, pouvant intervenir dans n’importe quelle cellule).
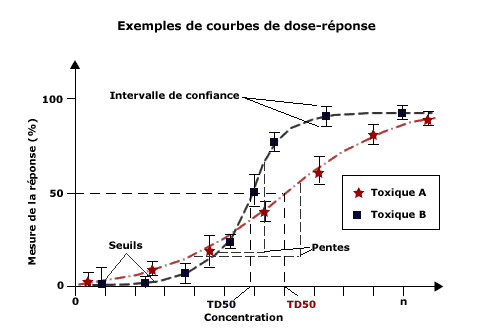
En conséquence, l’étude toxicologique s’attache à caractériser un certain nombre de paramètres quantitatifs, dont un est représenté sur la figure. Il s’agit de la TD50 ou dose toxique 50, qui représente la dose ou la concentration du toxique qui provoquent l’effet délétère étudié chez 50% des sujets. D’autres sont dérivés de l ‘ensemble des points expérimentaux, le plus important étant la dose sans effet nocif observable ou DSENO. Celles-ci est l’entité à partir de laquelle sont établies les valeurs toxicologiques de référence ou VTR
Remarque
Il existe deux façons d'exprimer le risque à partir des VTR :
- Dans le cas d'une toxicité avec seuil d'effet, le coefficient de danger (QD) (appelé aussi parfois indice de risque) exprime le rapport entre la dose effectivement reçue (par unité de temps, journalière par exemple) et la dose de référence (dose journalière admissible par exemple). Plus la valeur est supérieure à 1, plus le risque est probable.
- Pour calculer l'excès de risque individuel ou ERI (effets sans seuil), il faut connaître l'ERU qui correspond au nombre de cas supplémentaires pour une dose donnée et une exposition vie entière (typiquement 70 ans) et la dose reçue par l'individu (concentration et durée d'exposition) extrapolée vie entière.
Des paramètres qualitatifs seront aussi issus de l’étude toxicologique, en particulier en ce qui concerne le type de toxicité, les organes atteints et les délais d’apparition des manifestations. Cette notion de délais permet de distinguer les effets aigus, qui apparaissent dans la foulée d’une exposition, généralement à forte dose, des effets chroniques, qui peuvent se manifester longtemps après (en mois ou années), généralement suite à des expositions répétées et à plus faible dose.
Un recueil des méthodes expérimentales validées, utilisables pour l’évaluation de la toxicité des substances chimiques est disponible sur le site de l’OCDE. Il est assez exhaustif et est mis régulièrement à jour.
L’expologie fait le lien entre la présence d’une substance toxique dans l’environnement et l’apparition du dommage
La nécessité de mesurer l’exposition a été clairement présentée lors de la distinction faite entre dangers et risques. Obtenir une estimation de l’exposition à l’échelle d’un groupe ou d’une population n’est pas sans poser un certain nombre de problèmes méthodologiques. Ceux-ci sont parfois d’ordre métrologique. En matière de pollution, des campagnes (ponctuelles) ou des réseaux (permanents) de mesures peuvent être mis en place en fonction de la disponibilité d’indicateurs de ce que l’on cherche à mesurer.. Il reste malgré tout la difficulté d’associer un niveau de pollution en un lieu donné avec une population étudiée qui sera considérée comme exposée au niveau mesuré. En prenant l’exemple de la pollution atmosphérique on comprend aisément que l’association n’est pas si simple, car les individus composant la population, ont tous un comportement (au cours d’une journée) différent [Le terme savant utilisé est celui du budget espace-temps], ce qui peut influencer le niveau d’exposition. En conséquence, la mesure du niveau d’exposition doit se faire au plus près, sachant qu’il est très difficile d’obtenir des indicateurs parfaits.
Cette difficulté peut être contournée grâce à l’utilisation des
biomarqueurs. Ceux-ci sont mesurés par des dosages dans les liquides corporels ou les tissus. Les substances recherchées sont les polluants eux-mêmes (les toxiques) ou leurs métabolites [Dérivés de la substance initiale après transformations dans certains tissus, principalement le foie.]. Dans ce cas la concentration d’un biomarqueur est le reflet exact de l’exposition individuelle et intègre certains facteurs de variabilité (
susceptibilité individuelle ou efficacité d’absorption par exemple). La mesure de l’exposition en milieu professionnel permet d’illustrer l’importance des biomarqueurs, un niveau élevé pouvant être un élément clé dans la détermination d’une pathologie d’origine professionnelle.
L’épidémiologie s’adresse directement à l’état sanitaire des populations et à leurs causes
Sur le plan étymologique, l’épidémiologie est la discipline (logos) qui étudie l'influence de divers facteurs sur (epi-) des populations (demos=cité). Elle est issue des démarches de santé publique pour combattre les épidémies et les affections d'origine infectieuse au 19ème siècle. Mais la reconnaissance de l'influence du milieu remonte à l'origine de la médecine.
Complément
Hippocrates : "Sur les airs, eaux et endroits..."
Quiconque souhaite étudier convenablement la médecine, devrait procéder ainsi : tout d'abord il devrait considérer les saisons de l'année car leurs effets ne sont pas du tout semblables, mais diffèrent beaucoup entre elles par rapport à leurs changements. Puis les vents, les chauds et les froids, en particulier ceux qui sont communs à tous les pays et aussi ceux qui sont propres à une localité. Nous devons encore considérer la qualité des eaux...
Traduction approximative
L'ensemble des champs couverts par la santé publique repose sur les données épidémiologiques.
L'
épidémiologie descriptive nous fournit les indicateurs de l'état sanitaire d'une population, éventuellement standardisés pour s'affranchir de certains facteurs de variabilité. Nous pouvons ainsi mesurer l'
incidence et la
prévalence d’une maladie et calculer les taux spécifiques par tranche d'âge et par sexe. Nous pouvons alors aborder la recherche de liaisons avec une exposition, une pratique, un lieu de résidence, la profession. C'est l'objet de l'
épidémiologie analytique, appelée aussi étiologique, car elle essaye de rechercher des causes.
Pour simplifier la présentation, dans une étude analytique on constitue deux groupes. Le premier est constitué d’individus atteints d'une pathologie donnée (troubles respiratoires, allergies ou cancers, pour prendre quelques exemples), c’est las cas. Le second comprend des individus sains (qualifiés detémoins). Le but est d’étudier l’exposition à un facteur supposé de risque (exposition, mode de vie etc.), qui se répartirait différemment chez les cas et les témoins. Il est capital que les deux groupes soient comparables pour toutes les caractéristiques (démographiques ou socioprofessionnels par exemple), sauf le facteur étudié, sinon les conclusions risquent d’être faussées. On évoque alors l’existence de biais ou de facteurs de confusion, dont il faut tenir compte dans l’exploitation des résultats. Quatre groupes résultent de cette analyse, permettant le calcul de deux proportions ou rapports, dont la comparaison fournira une indication du lien entre le facteur de risque et la pathologie. Le rapport des rapports appeler risque relatif (souvent représenté par l’entité “odds ratio”), accompagné d’un intervalle de confiance donne la mesure quantitative du risque.
Synthèse des différents apports : caractérisation des risques sanitaires
Après avoir présenté les spécificités des trois domaines disciplinaires, il faut examiner de quelle manière les différentes informations s’articulent dans le but d’évaluer les risques sanitaires. Chaque information a son importance et fournit, in fine, aux décideurs publics les éléments nécessaires pour gérer le risque.
Les études épidémiologiques portent directement sur l’influence des facteurs de risque sur la santé des populations. De ce point de vue, elles constituent le plus haut niveau de preuve dans un dossier concernant le facteur de risque. Mais l’épidémiologie ne nous apporte des indications que sur une association : exposition -> augmentation de la fréquence d’une pathologie. Elle n’offre aucune indication quant au mécanisme d’action qui doit être étudié séparément, dans des modèles appropriés. De plus, elle ne contribue que rarement des données pour établir les relations exposition – effets.
La connaissance du mécanisme d’action est-elle indispensable ? Pour renforcer le lien causal entre les manifestations pathologiques et l’exposition à un déterminant environnemental il faut que l’apparition d’un trouble soit compatible avec ce que l’on sait du mécanisme d’action. Ceci renforce la plausibilité de ce qui est autrement une simple observation. Il existe d’autres règles permettant de renforcer la causalité, la principale étant celle de la relation temporelle qui impose qu’il y ait exposition avant que n’apparaissent les symptômes de la maladie.
Pour résumer les différents apports :
-
La toxicologie permet de définir le type de toxicité et de fournir une relation de dose – réponse. Elle utilise des modèles, ce qui nécessite d’étudier les conditions de la transposition, par exemple de l’animal à l’homme.
-
L’expologie étudie l’exposition à un déterminant donné, à l’échelle de la population. Elle offre une image de l’étendue du problème que les mesures de gestion devraient pallier.
Une fois que le niveau d’exposition a été obtenu, il peut être transformé en risque de développer une pathologie grâce à une fonction dose – réponse. Ces fonctions sont fournies par les études toxicologiques sur les modèles animaux ou des cellules en cultures. La transposition de l’animal à l’homme se fait avec l’application de facteurs d’incertitudes plus ou moins standardisés.
-
L’épidémiologie étudie la corrélation entre l’exposition et le développement d’une maladie en situation réelle. A elle seule (en cas de résultat positif) elle constitue une indication de l’existence d’un risque. Par contre, associée aux données toxicologiques, les résultats des études épidémiologiques apportent la preuve ultime et fournissent la meilleure estimation quantitative du risque [Celle-ci comporte toujours des incertitudes, ne serait-ce que par l’intervalle de confiance du risque relatif calculé].
Typologie des situations à risques et comment y pallier
L'intérêt des classifications
La classification des déterminants environnementaux en fonction de leur nature, physique, chimique ou biologique, est la plus utilisée. Elle est pertinente à plus d'un titre :
-
Elle renseigne sur les sources (les rayonnements par exemple) ;
-
Elle fourni des indications sur le mode de propagation (vecteurs biologiques ou rayonnements) ;
-
Elle est utile pour définir les mesures de protection (les modes d'exposition aux substances chimiques sont fondamentalement différents de ceux des rayonnements ou du bruit).
Cette classification est présente dans tous les documents officiels. Néanmoins, pour se fixer des objectifs, en particulier pour atténuer ou prévenir les impacts sur la santé et l'environnement, bien d'autres classifications s'avèrent utiles. Dans le cas des déterminants biologiques nous pouvons distinguer les bactéries des virus. Mais c'est pour l'énorme diversité des substances chimiques que les critères de classification seront les plus utiles.
Les propriétés physicochimiques sont à la base d'une classification de dangerosité et de l'association avec les phrases de risque (irritant, corrosif, inflammable, etc.). Les facultés de persistance et de
bioaccumulation sont essentielles pour la caractérisation de la toxicité environnementale, qui peut avoir des conséquences indirectes sur la santé de l’homme. Citons encore la classification des types de toxicité : par exemple, neurotoxique, toxique pour la reproduction ou cancérigène, dont l'intérêt se retrouve dans les mesures de protection, éventuellement aggravées pour des populations sensibles.
Bien d'autres critères “opérationnels” peuvent trouver des applications spécifiques : par exemple pour faciliter l'élaboration de mesures, de “guidelines”, de préconisations, de prescriptions contraignantes, dans le but de protéger l'utilisateur, le consommateur et l'environnement. Leur présentation dépasse le cadre d’un cours introductif.
Exemples de conséquences sanitaires dues à des déterminants environnementaux
Facteurs physiques : Les rayonnements et le bruit sont des exemples de facteurs physiques ayant des impacts sanitaires. Les rayonnements ionisants (Rayons X ou gamma) sont cancérigènes, comme le sont aussi les rayonnements UV, dont la capacité de pénétration est plus faible et se limite à des effets sur la peau. Quant au bruit, les conséquences sont multiples et beaucoup plus difficilement mesurables, car la perception de l’environnement sonore et même le type de bruit ou encore le moment dans la journée, peuvent jouer sur les résultats.
Les rayonnements ionisants sont des cancérigènes puissants, mais la population exposée n’est pas nombreuse (sauf pour certaines professions). Le cas du radon, un gaz radioactif produit de la décomposition de l’uranium, mérite une mention spéciale. Certaines roches, utilisées dans la construction de logements, en émettent suffisamment pour que la concentration dans l’air intérieur atteigne des niveaux pouvant causer un nombre significatif de cancers du poumon. L’exposition au soleil (rayonnements UV) est le principal facteur de risque des 6000 nouveaux cas de
mélanome observés en France. Enfin, pour ce qui concerne le bruit, avec toutes les précautions nécessaires compte tenu des difficultés mentionnées précédemment, des populations très importantes sont exposées à des niveaux qui dépassent les seuils préconisés par l’OMS [65% de la population européenne serait exposée à des niveaux supérieurs à 55 dBA leq sur 24 heures – seuil définissant la gène sonore selon l’OMS (source OCDE).].
Dans les facteurs biologiques, celui qui est cité le plus souvent concerne les légionelles, bactéries responsables d’une infection respiratoire le plus souvent bénigne (environ 95% des cas.. Les légionelles vivent en milieux hydriques à une température optimale entre 25 et 45 °C. L’homme s’infecte en inhalant un aérosol d’eau contaminée, ceux émis par les tours aéro-réfrigérantes, résidentielles ou industrielles.
Facteurs chimiques : Les risques associés aux substances chimiques sont ceux qui focalisent le plus l’attention. Etant donné le nombre de substances concernées (plus de 100000 enregistrées dans la base de données européenne pour les substances mises sur le marché avant 1981), utilisées dans de nombreux procédés industriels et rentrant dans la composition d’innombrables produits de consommation, l’évaluation des risques correspond à une tâche colossale. C’est la raison même de l’adoption du nouveau règlement REACH par l’UE.
Les conséquences de l’exposition aux fibres d’amiante (300 000 morts sur la période 2000-2025), largement médiatisées, fournissent une bonne illustration. Il en existe d’autres. Par exemple l’augmentation de l’incidence de certains cancers autour des usines d’incinération d’ordures ménagères, attribuée à la présence d’un fort taux de dioxines dans les fumées. Dans d’autres cas nous connaissons l’exposition, mais comme les pathologies sont multifactorielles, le nombre de cas attribuable reste théorique. Ainsi, en France, environ 2 370 000 de travailleurs étaient exposés en 2003 à des agents cancérogènes, mutagènes ou reprotoxiques [Toxique pour la fonction reproductive]. A l’échelle européenne et pour les niveaux d’exposition connus, environ 4% des cancers devraient être attribués au milieu professionnel. A minima, environ 2600 cas sont réellement reconnues d’origine professionnelle, dont 70% pour l’amiante.
Les
pesticides sont également une source de préoccupation. Cette très large catégorie de substances comprend des cancérigènes, des neurotoxiques, des toxiques pour la reproduction. Du point de vue santé publique, on commence à peine à mesurer l’étendue des dégâts encore une fois en milieu professionnel, c’est-à-dire principalement chez les agriculteurs. L’augmentation des symptômes neurologiques, révélée dans certaines études en cours (AGRICAN ou PHYTONER par exemple), constitue clairement une source de préoccupation. Des cas de maladies neurodégénératives commencent aussi à être reconnus comme ayant une origine professionnelle (applicateurs de pesticides).
L’importance des circonstances d’exposition.
Cette approche basée sur les éléments du contexte à été proposée par l’UE. Trois types de situations sont identifiées :
-
Les expositions volontaires, comme c’est le cas pour la mise sur le marché et l’utilisation de substances dangereuses, dès lors que leur utilité est établie et que des mesures appropriées sont identifiées pour minimiser tout risque. Typiquement, dans le cas d’une exposition volontaire, la procédure mise en œuvre est celle de l’évaluation des risques sanitaires : l’exposition doit être maîtrisée, dans le but de protéger le professionnel ou l’utilisateur. La définition de la procédure de contrôle (mesures réglementaires, préconisations ou restrictions d’usage) fait partie de la gestion du risque. Les produits phytosanitaires et les autres biocides font l’objet de telles procédures et sont réglementés par des directives spécifiques.
-
Les expositions involontaires, occasionnées au cours d’une activité ou d’un procédé, dont l’exemple-type est la pollution due au trafic automobile. Pour les expositions involontaires il faut pratiquer une évaluation des dommages sanitaires qui nécessite de déterminer les niveaux d’exposition, d’étudier l’état sanitaire de la population, puis de corréler les deux. Ainsi, il sera établi si les niveaux des polluants réglementés respectent les préconisations internationales (celles de l’OMS par exemple), s’ils sont compatibles avec la garantie d’une bonne santé pour la population.
-
Les expositions accidentelles constituent un cas à part. Elles sont considérées autour d’installations industrielles classées pour l’environnement (ICPE), qui appartiennent à une liste pré-établie en fonction des dangers intrinsèques à leur exploitation. Cette réglementation a été mise en place suite à l’accident de Seveso (incendie provoquant des émanations très importantes de dioxines). Dans ce cas, ce n’est plus seulement le risque qui est visé mais aussi le danger. Outre les mesures de prévention de l’accident, l’exploitant a l’obligation de traduire dans un document validé par les services de l’état, les moyens mis en œuvre pour limiter les dommages en cas d’accident.
Conclusion
Tout au long du cours nous avons présenté les éléments clés pour la bonne mise en œuvre de l’expertise scientifique en appui à la décision publique. Si le contexte a été progressivement améliorer sur le plan méthodologique, malgré les progrès continus dans les connaissances, des controverses surgissent en permanence du fait de l’extrême complexité des domaines concernés. La communauté scientifique se doit de faire le point sur l’état des connaissances du moment, avec leurs lacunes identifiées, en rapport avec la question posée et à laquelle il n’est pas toujours possible de répondre de façon satisfaisante. Les évaluations scientifiques doivent intégrer l'information allant de l’ensemble de connaissances scientifiques bien établies aux conjectures intuitives, aux modèles préliminaires, aux hypothèses expérimentales, l’ensemble étant susceptible d’évoluer avec de nouvelles connaissances. Ainsi la décision publique, pour gérer le risque, comportera une part d’anticipation (décisions prises dans le sens de la précaution sur la base de dommages potentiels importants et de données scientifiques présentant de fortes incertitudes). De même elle peut intégrer une part d’adaptation programmée, correspondant aux questions en suspens n’ayant pas donner lieu à une décision, mais susceptibles de l’être en fonction de l’évolution des connaissances.